Fisika-Kimika»Fisika - Kimika
Kimika eta bizitza arrunta
Airea
Lurra inguratzen duen gas geruza da airea. Ezin da haren lodiera zehaz-mehatz jakin, baina, gutxi gorabehera, lurretik 500 km-ra behar du izan muga, handik aurrera atmosfera kosmikoa hasten dela onartzen baita. Pisua, berriz, 5,3 bilioi tona ingurukoa du. Eguratsa, bestalde, ez dago substantzia bakar batez osatua, hainbatez baizik, gas nahaste bat baita:

Gas horiez gainera, autoek eta industriek botatzen dituzten gasak eta era askotako partikulak (aerosolak) daude airean suspentsioan: hautsa, mikrobioak, sufre dioxidoa, ozonoa
Aireak (urak bezalaxe) sekulako garrantzia du prozesu biologikoetan. Airerik ezean minutu gutxitan hilko lirateke lurreko izaki bizi gehienak. Eguratsak badu, gainera, beste zeregin nagusi bat: espaziotik iristen diren irrada kosmikoetatik babestea eta tenperatura aldaketa handiak eragoztea.
Aireak, oxigenoa izanik, erreakzio kimiko askotan parte hartzen du (errekuntza, oxidazioa eta abar).
Eguratseko gasak eskuratzeko modu bat baino gehiago dago. Industrian, adibidez, destilazio zatikatua erabiltzen da; batez ere oxigenoa eta nitrogenoa eskuratzen dira horrela. 1895. urtean Karl Ritter von Linde (1842-1934) alemaniar asmatzaile eta industria gizonak airea isurkari bihurtzeko sistema bat aurkitu zuen, Joule- Thomson efektua aplikaturik.

Joule-Thomson efektuaren eskema

Amoniakoaren Haber prozesua burutzeko lantegia
Industrian, amoniakoaren sintesian eta kriogenian erabiltzen da nitrogenoa (irakite puntua: -197,5 °C). Amoniakoa garrantzi handikoa da ongarri nitrogenodunak lortzeko. Airea isurkari bihurtu eta gero destilatuz, nitrogenoa lortu ondoren, hidrogeno hutsarekin nahasten da. Nahasketa hori tenperatura handian (500-600 °C) eta presio handian (100-1.000 atm) hodi batzuetan zehar igaroarazita amoniakoa lortzen da.

Kriogenia, berriz, oso tenperatura hotzak lortzeko teknikak eta oso tenperatura hotzetan izaten den jokaera aztertzen dituen fisikaren alorra da. Kriogenia garrantzi handikoa da metalek tenperatura hotzetan duten portaera ezagutzeko. Adibidez, eroamen elektrikoa eta termikoa tenperatura txikietan oso handia izan daitekeela jakin da kriogeniaren bidez (material supereroaleak). Elikagaiak kontserbatzeko ere asko erabiltzen da (elikagai ultraizoztuak).
Oxigenoa ere (irakite tenperatura: -182,5 °C) airetik lortzen da. Oxigeno garbia gero eta gehiago erabiltzen da industrian, siderurgian (Martin-Siemens labeetan edo Lind-Donowitz trukatzaileetan, esate baterako). Austronautikan ere garrantzi handia du, erregai gisa erabiltzen baita.
Jakiak 0-5 °C bitarteko tenperaturan direnean, bakterio eta gainerako mikrobioen jarduera guztiz gelditzen ez bada ere asko mantsotzen da. Etxean-eta, horregatik gordetzen dira elikagaiak hozkailuan, egun gehiago iraun dezaten jateko moduan. Epe luzeetarako, baina, 0 °C azpitik izoztu behar dira, mantenduko badira.
Jakiak -40 °C-tan izozteari ultraizoztea esaten zaio. Izoztu ondoren, aski da -20 °C-tan edukitzea jakiak bere itxura eta propietateak gorde ditzan. Zer gorabehera dago ordea jaki bat tenperatura batean ala bestean izoztuz gero? Kontua da, jakia tenperatura apal-apaletan izoztuz gero, oso izotz kristal txikiak eratuko direla, eta hala, hura desizoztean eta kristal txikiak urtzean, jakiaren barne egitura eta tasunak ia ez direla aldatuko.
Eguratsaren kutsadura
Gauza jakina da gizakiaren zenbait jarduera oso kalteagarria izan dela eta izaten ari dela gaur egun ere eguratsarentzat. Azkeneko urteotan askotan apurtu da gasen arteko oreka eguratsean, eta kolokan jarri da izaki bizidunen iraupena lurrean. Hitz berriak ere asmatu dira, kutsadura dela eta; smog hitza, adibidez, ingeleseko smoke eta fog hitzen bat egitea da, eta hiri handi batzuetan izaten den ke lainoa adierazteko erabiltzen da.
Anhidrido karbonikoaren kantitatea eguratsean %15 handitu da XX. mendean zehar, ikatzaren errekuntzagatik batez ere. Urtero %0,4 inguru handitzen da. Anhidrido karbonikoa kristal izpiak balira bezala da eguzki izpientzat, eta horrek eguratsean duen ondorioari (egurats berotzeari, alegia) berotegi efektua esaten zaio.

Berotegi efektuak planetaren tenperatura igotzea eragin lezake, eta horrek sekulako ondorio kaltegarriak izan ditzake: lurburu inguruko izotza urtzea eta itsaso maila igotzea, itsas herri eta hiri asko urpean gelditzea, eta abar.
Kutsaduraren beste eragile nagusietako bat freoia da. Gas geldoa da freoia,
aerosoletan-eta oso erabilia 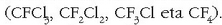 Eguratsean dagoenean deskonposatu egiten da eguzki izpien eraginez, katea erreakzio bat eragiten du orduan,
eta atmosferako ozonoa deskonposatzen du. Eta ozonoaren zeregin nagusia lurra eguratsean sartzen
diren izpi kaltegarrietatik babestea da.
Eguratsean dagoenean deskonposatu egiten da eguzki izpien eraginez, katea erreakzio bat eragiten du orduan,
eta atmosferako ozonoa deskonposatzen du. Eta ozonoaren zeregin nagusia lurra eguratsean sartzen
diren izpi kaltegarrietatik babestea da.
Ozonoa ordea, argi ultramorea absorbaturik, oxigeno atomo eta molekula banatan deskonposatzen da. Beraz, halako oreka bat dago prozesu horien artean. Ozono geruzak izpi ultramoreetatik babesten du lurra, zelula bizientzat kaltegarri baitira. Ozonorik ezean ezinezkoa izango litzateke lurrean bizia. Ozonoa gutxitzeak, adibidez, larruazaleko minbizia areagotzea ekarri du.
Troposferan ozono asko izatea kaltegarria baldin bada (gogoan izan smog fotokimikoa), are kaltegarriagoa da oraindik ozono gutxi izatea. Egiaztatu ahal denez, ozonoa urritzearen eragileen artean aerosol eta hozkailuetako klorofluorometanoak (freoia) dira nagusiak. Gai horiek ez dute, nonbait, eguratsaren beheko geruzetan erreakzionatzen, bai ordea, estratosferan, irrada ultramoreen eraginez:

Kloro atomoek ozonoaren deskonposatzea katalizatuko dute:

Eta kloro atomoak berriro askatzean, erreakzio hau gertatzen da:
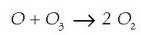
Horiek dira segur aski eguratsa kutsaduraren gertaera ezagunenak. Gaur egun, pixka bat bada ere, egoera aldatzen ari da. Legeak oso zorrotz kontrolatzen ditu orain industrien gas jarioak. Industria asko beste era batera diseinatu behar izan dira kutsadura murrizteko, gutxiago kutsatzen duten gasolinak prestatu dira (berunik gabeko gasolina), eta abar. Argi dago industriak sortzen dituen arazo asko konpon daitezkeela nahi izanez gero. Londres hiriko eguratsa, adibidez, askoz garbiagoa dago gaur egun 60ko hamarraldian baino. Halako zerbait gertatu da Rhin ibaiarekin ere.
Zer kutsadura mota adierazten du smog hitzak? Klima hezeetan ikatzaren
errekuntzan sortzen den ke eta sufre dioxidozko nahastea, hain zuzen. Bai, gaur egun, smoga
gutxitzen ari da, ikatz gutxiago erretzen baita, baina, aitzitik, gero eta zabaltzenago ari
da smog fotokimikoa. Smog fotokimikoa, horrela esaten baitzaio ingurune eguzkitsuetan auto
eta gainerako ibilgailuetako gasek eragiten duten kutsadura moduari. Smog fotokimikoaren
jatorria oso-oso garbi ez badago ere, nitrogeno eta oxigenoaren arteko konbinazioz sortzen
dela uste da. Nitrogeno geldoak eta oxigenoak tenperatura handitan erreakzionatzean NO sortuko da.
Eguratsean dagoen bitartean oxigenoarekin oxidatuz joango da pixkaka eta
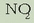 bihurtuko da.
Batzuetan,
bihurtuko da.
Batzuetan,  -ren
kontzentrazioa oso handia denean, kolore horixka-gorrixkako geruza moduko bat eratzen da.
-ren
kontzentrazioa oso handia denean, kolore horixka-gorrixkako geruza moduko bat eratzen da.
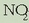 -ren
kontzentrazioa ez da normalean oso handia izaten, eta kutsadura ez da berehala edo zuzenean antzematen.
Ez,
-ren
kontzentrazioa ez da normalean oso handia izaten, eta kutsadura ez da berehala edo zuzenean antzematen.
Ez,  -ren ondorio
kaltegarria beste modu batzuetan azaltzen da: euri azidoan adibidez. Euri azidoaren eragileetako bat da.
Argi ultramorearen eraginez, bestalde, deskonposatu egiten da, eta NO eta oxigeno atomoak ematen ditu:
-ren ondorio
kaltegarria beste modu batzuetan azaltzen da: euri azidoan adibidez. Euri azidoaren eragileetako bat da.
Argi ultramorearen eraginez, bestalde, deskonposatu egiten da, eta NO eta oxigeno atomoak ematen ditu:

Oxigeno atomikoa oso ezegonkorra da, eta ozonoa ematen du oxigeno molekularrarekin erreakzionatzean:
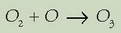
Ozonoaren ahalmen oxidatzailea oso handia denez, kaltea eragiten du zenbait gauzatan (kautxua, pintura, landaredia ), eta begietako azkura eta biriketako arazoak sor ditzake besteak beste.
Smogak oso kalte larriak eragin ditu Los Angeles hirian (Estatu Batuak), hartarako baldintza guztiak betetzen baitzituen, alegia, auto asko eta beraz kutsadura handia izatea, klima eguzkitsua izatea eta abar. Smogaren arazoa dela eta, azkeneko urteotan aurrerapen handiak egin dira automobilaren industrian, baina, nolanahi ere, arazoa behin betiko desagerrarazteko modurik hoberena gertaera bera ez gertatzea da.
Ozono geruza
Estratosferako osagai nagusietako bat da ozonoa. Eguratsean,
15-25 km artean, 10 ppm-koa da ozonoaren kontzentrazioa
(troposferan, berriz, 0,04 ppm ingurukoa). Eguzkiaren izpi ultramoreek
oxigenoa 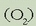 deskonposatzean sortzen da ozonoa.
deskonposatzean sortzen da ozonoa.

Lurretik 200 km-ra presioa eta oxigeno atomoen kontzentrazioa txikiak direnez, nekez konbinatzen dira oxigeno atomoak oxigeno molekulak osatzeko. Baina oxigeno atomoak beherago sortzen direnean, berehala elkartzen dira oxigeno molekulekin ozonoa emateko:
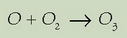
Euri azidoa
Ibilgailuak, industria prozesuak, zentral termikoak etab. direla eta, asko handitu da azkeneko
urteotan erregai fosilen kontsumoa (ikatza eta petrolioa batez ere); sufre eta nitrogeno oxido
asko bota da eguratsera, eta hala, euri azidoaren arazoak okerrera egin du. Izan ere, eguratsera
botatako gai horietatik substantzia azidoak sortzen dira, eta euria egiten duenean, lurrera erortzen
dira urarekin batera. Hormategi eta bestelako izoztegietako pH-a neurtuta, duela berrehun bat urte
eroritako euria neutro samarra zela (6-7,6) jakin ahal izan da. Gaur egun, ordea, ipar hemisferioan
egiten duen euriaren pH-a 4-4,5 ingurukoa da. Egoera askoz okerragoa da leku jakin batzuetan:
Estatu Batuetan, Wheeling hirian (Mendebaleko Virginia), euriaren azidotasuna izugarria da batzuetan
(1,5 ingurukoa); Los Angeles inguruan normala da lainoak 2,2-4,0 arteko pH-a izatea. Gorago aipatu
den bezala, erregai fosilen errekuntza dela eta sufre eta nitrogeno oxido asko
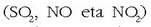 igortzen da eguratsera,
eta eguratseko oxigenoarekin eta ur lurrunarekin erreakzionatzean, azidoak sortzen dituzte: azido sulfurikoa
eta azido nitrikoa, hain zuzen. Egia esan, eguratsean den sufre oxidoaez da soilik industrian sortua,
bai baita jatorri naturala duenik er e (sumendiek, adibidez, anhidrido sulfurosoa botatzen dute erupzioan;
bakteria anaerobikoen metabolismoan eta hainbat prozesu biologikotan ere anhidrido sulfurosoa sortzen da).
Are gehiago, jatorri naturala duen
igortzen da eguratsera,
eta eguratseko oxigenoarekin eta ur lurrunarekin erreakzionatzean, azidoak sortzen dituzte: azido sulfurikoa
eta azido nitrikoa, hain zuzen. Egia esan, eguratsean den sufre oxidoaez da soilik industrian sortua,
bai baita jatorri naturala duenik er e (sumendiek, adibidez, anhidrido sulfurosoa botatzen dute erupzioan;
bakteria anaerobikoen metabolismoan eta hainbat prozesu biologikotan ere anhidrido sulfurosoa sortzen da).
Are gehiago, jatorri naturala duen  -aren
kantitatea gizakiak sortzen duena baino bi aldiz handiagoa da. Nolanahi ere, gizakiak sortzen duenak
askoz ondorio kaltegarriagoak ditu: jatorri naturala duen anhidrido sulfurosoa homogeneotasunez banatua
dago lurrean, eta industrian sortzen dena, berriz, leku jakin batzuetan pilatzen da gehiena
(40 eta 60 ºko latitudeen artean, adibidez, Europan).
-aren
kantitatea gizakiak sortzen duena baino bi aldiz handiagoa da. Nolanahi ere, gizakiak sortzen duenak
askoz ondorio kaltegarriagoak ditu: jatorri naturala duen anhidrido sulfurosoa homogeneotasunez banatua
dago lurrean, eta industrian sortzen dena, berriz, leku jakin batzuetan pilatzen da gehiena
(40 eta 60 ºko latitudeen artean, adibidez, Europan).
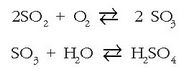
Euria egiten duenean azido sulfurikoa urarekin batera erortzen da eta horrexegatik esaten zaio euri horri euri azidoa.
Errekuntzan izaten diren tenperatura handiek aireko nitrogenoaren eta oxigenoaren arteko
erreakzioa eragin dezakete (tenperatura txikietan nitrogenoa gas geldoa da), eta NO eta
 gasak eman.
Oxido horiek azido nitriko bihur daitezke hezetasunaren laguntzaz.
gasak eman.
Oxido horiek azido nitriko bihur daitezke hezetasunaren laguntzaz.
Zer nolako eragina du euri azidoak lurrean?
Euri azidoak oso eragin kaltegarria du izaki bizidunetan, landareetan batez ere. Landareen fotosintesia galarazten du, likenak murrizten ditu eta landareen hostoak deusezten ditu. Euri azidoa dela eta Alemaniako Errepublika Federaleko basoen %7 alferrik galdu zen 1982an. Animaliei ere sufre dioxidoak (SO2) arazoak sortzen dizkie arnasbideetan. Arazo horiek handiagoak dira hezetasun handiko inguruneetan.
Euri azidoak ez ditu lur mota guztiak berdin erasaten. Karezko lurrak, adibidez, azidotasuna neutralizatzeko gai baitira, ez ditu hainbeste erasaten:
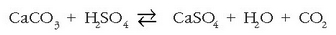
Silikatozko lurretan ordea ez da halako neutralizaziorik eta euri azidoaren eragina askoz handiagoa da. Euri azidoak, gainera, disolbatu egiten ditu aluminiozko konposatuak, eta urak berekin eramatenditu antziretaraino. Hori dela eta, asko handitzen da Al toxikoren kontzentrazioa uretan, eta hil egiten dira arrainak (horixe gertatu da Suedia eta Norvegiako 20.000 bat antziretan).
Beste arazo larri bat irispidearena da; euri azidoak ez du zertan sortu den lekuan erori, eta herrialde batean sortzen den kutsadura kutsadurarik sortzen ez duen beste batera hel daiteke. Suedian urtetan erori den euri azidoa Britaina Handian sortu ote den susmoa dago. Antzeko zerbait gertatu da Estatu Batuen eta Canadaren artean, eta batak besteari leporatzen dio euri azidoa sortzearen erantzukizuna.
Izaki bizidunetan ez ezik gauza eta materialetan ere kalte handia eragiten du euri azidoak. Kare harriz eta marmolez egindako eraikuntza historiko asko, adibidez, euri azidoak higaturik daude.

Euri azidoaren eraginez, eraikuntza batean urte gutxitan gertatutako higadura
Zer egin euri azidoaren aurka?
Euri azidoaren jatorria ikusirik eta datozen urteetan energia eskaria gutxituko ez denez,
sufre gutxi sortzen duten erregaiak erabili beharko lirateke; ikatza haustuta
(burdina sulfuroa edo pirita  -
desagertzeko) erabili beharko litzateke eta fuel-olioa kaltzio oxidoarekin (CaO) tratatu. Sufre gutxiago
sortzeko beste bidebat errekuntza prozesua bera hobetzea izango litzateke. Ikatza eta kare harria
-
desagertzeko) erabili beharko litzateke eta fuel-olioa kaltzio oxidoarekin (CaO) tratatu. Sufre gutxiago
sortzeko beste bidebat errekuntza prozesua bera hobetzea izango litzateke. Ikatza eta kare harria
 batera
eta lastertasun handiko airea erabiliz erretzen badira, tenperatura ez da 800-900 °C-tik gora igotzen.
Baldintza horietan oso nitrogeno oxido gutxi sortzen da, eta, gainera, sufre dioxidoa kare harritik datorren
kaltzio oxidoarekin erreakzionaten du.
batera
eta lastertasun handiko airea erabiliz erretzen badira, tenperatura ez da 800-900 °C-tik gora igotzen.
Baldintza horietan oso nitrogeno oxido gutxi sortzen da, eta, gainera, sufre dioxidoa kare harritik datorren
kaltzio oxidoarekin erreakzionaten du.
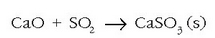
Modu honetan atmosferara botatako  gasaren kantitatea %90ean gutxitzea lortu da.
gasaren kantitatea %90ean gutxitzea lortu da.
Koloregaiak
Zerbait koloreztatzeko erabiltzen diren gaiak dira koloregaiak, eta aspalditik erabiltzen dira. Fenizioek zenbait soinberaren tinta erabiltzen omen zuten ehunak-eta tindatzeko. Koloregai sintetikoak 1856. urtean hasi ziren erabiltzen, William Perkin ingeles kimikariak (1838-1907) anilinatik eratorritako lehen koloregai sintetikoak aurkitu zituenean. Handik aurrera etengabe aurkitu dira koloregai mota berriak eta hobeak. 1868an alizarina sintetizatu zen eta 1880an indigoa. Koloregai modernoen artean aipatzekoak dira erreaktiboak. Erreaktiboek gaiari kolorea emateaz gainera harekin erreakzionatzen dute eta molekula berriak sortzen dituzte. Era horretako lehenengo koloregaiak, Procion eta Cibacrom, ICI eta CIBA konpainiek merkaturatu zituzten, hurrenez hurren. Biak koloregai azidoak dira eta bisulfato talde bat dute uretan disolbatu ahal izateko.
Beste laboratorio batzuek kloropirimidinazko taldeak dituzten koloregaiak lortu dituzte (Sandoz eta Geigy), edo 2-bentzotiazolaren eratorrietan oinarriturikoak: dikloro kinoxalinak, kinazolinak, etab. Azken urteotan koloregai nagusiak makromolekulak dira (talde kromoforoak dituzten molekula erraldoiak), edo metal konplexuak dituzten molekulak, bestela.
Pinturetan gehien erabiltzen diren pigmentuak gai ezorganikoak dira.
Pintura zurien artean titanio oxidoa 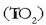 da gaur egun erabiliena
da gaur egun erabiliena
Kosmetikoak
Gorputzari edertzeko, zaintzeko, itxura aldatzeko, margotzeko, hezatzeko edo usain gozoa izateko ematen zaion gaia da kosmetikoa: koloniak, urrinak, perfumeak, ezpain margoak, makillajea, azazkal margoak, usain kentzaileak, xanpuak, ile tindatzaileak, etab.
Kosmetiko ezagunena beharbada urrina edo perfumea da. Urringileek loreetatik esentziak atera eta proportzio jakinetan nahastuz usain ederrak lortzen dituzte. Gaur egun urrinen industria izugarri zabaldu da, eta esentziak eta olioak landare eta loreetatik ez ezik laboratorioan sintesiz ere lortzen dira. Oso erabiliak dira, adibidez, estirenoa, geraniola, zitrala, etab.
Geraniola terpenoen familiakoa da; horiek dira landare eta lore gehienen usainaren eragileak. Landareetatik olio usaindunak lortzeko, landarea uretan destilatu behar da; destilatzean bereizten den olioak oso usain berezia izan ohi du. Laboratorioan terpenoak azido azetikotik abiatuz lortzen dira, isopentil pirofosfatoarekin erreakzionaraziz.
isopenil pirofosfatoa:
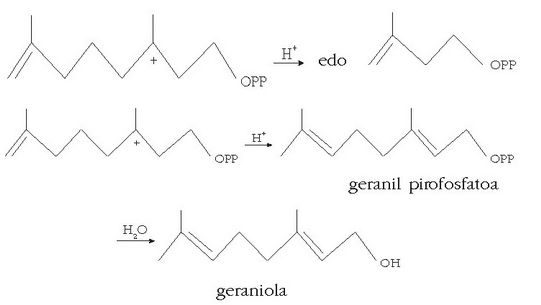
Asko erabiltzen den beste familia organiko bat esterrak dira: pamil azetatoa (banana usainduna), etil azetatoa (sagar usainduna), etab. Azido salizilikoa metanolarekin erreakzionaraztean metil salizilatoa sortzen da (gaulteria olioa), oso erabilia urrinen munduan.
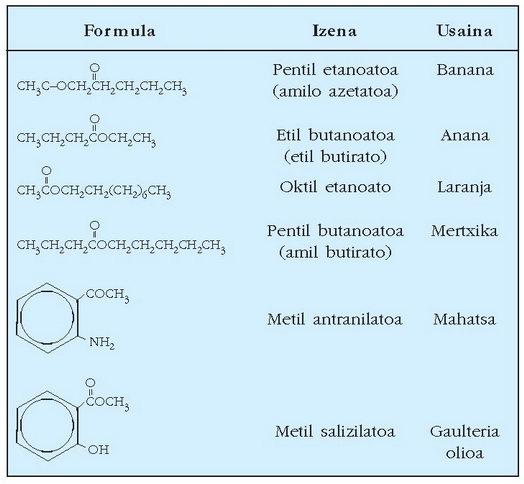
Gero, aukeratu den esentzia (natural edo sintetikoa) egoki nahastu ondoren urrina lortzen da. Hasieran kantitate txikitan prestatzen da laboratorioan, eta urrin edo kosmetiko egokia lortu ondor en, industrian ekoizten da. Produktu horiei beste gai bat erantsi ohi zaie finkatzailea, alegia, luzaroan gorde dezaten usain ona. Perfume normal batek 20 osagai izan ditzake. (Marrubiaren usaina, esate baterako, 250 gaik zehazten dute)
Kosmetikaren munduan apaingarriak izango dira segur aski alorrik garrantzitsuena eta ospetsuena. Apaingarrien osagai arruntenak baselina, parafina, lanolina, urrina, koloregaia eta argizaria dira, natural edo sintetiko
Ongarriak
Munduko biztanleria urriagoa zenean ez zen gaur adina arazo jendeak behar zituen elikagaiak lortzeko. Egun, ordea, arazo larria da hori, lurreko biztanleria izugarri handitu delako, batetik, eta lurra ez delako behar bezala zaindu, bestetik. Horrenbestez, nekazaritza hobeto kontrolatu behar izan da: lurraren kalitatearen arabera egokitu, hazi egokiak hautatu, ongarri hobeak erabili
Zer dira ongarriak?
Sail bat urterik urte uztak eman eta eman ari denean, elikagaia berritu behar zaio, landarea behar bezala haziko bada. Eta horixe da hain zuzen, ongarrien zeregina. Lehenago ongarri naturalak erabiltzen ziren; gaur egun, ordea, gero eta gehiago erabiltzen dira ongarri sintetikoak.
Hauek izaten dira ongarriaren osagai nagusiak: nitrogenoa (N), fosforoa (P) eta potasioa (K). Dituen osagai kopuruaren arabera bakuna, bitarra edo hirutarra izan daiteke.
Ongarri nitrogenoduna lortzeko iturri nagusitzat Chileko nitratoa erabili izan da urte askoan. Orobat erabili izan dira harrikatzaren alkaternaren gatz amoniakodunak eta karburo kaltzikoaren zianamina. Gaur egun ongarri nitrogenodunak lortzeko iturri nagusia amoniakoa da, laboratorioan sintetizatua (Haber-en prozesua). Ongarri nitrogenodunetan nitrogeno kantitatea %80 ingurukoa izan daiteke. Baserritarrek, bestalde, urea, amonio kloruroa eta amonio sulfatoa erabiltzen dituzte.
Fosforoa fosfato trikaltziko gisa dago izadian, eta landareek ezin dute horrela ongi asimilatu.
Hala, landareen elikatze prozesuan sartuko bada, uretan disolbatzea lortu behar da.
Horretarako erreakzioan sarrarazi behar da fosfato trikaltzikoa azidoren batekin
(azido nitrikoa, klorhidrikoa edo sulfurikoa) ur disoluzio batean. Industrian azido sulfurikoa erabiltzen
da gehienbat, eta lortzen diren gaiei superfosfato esaten zaie. Superfosfatoak fosfato monokaltzikoaren
eta dikaltzikoaren nahastea baizik ez dira (%20 inguru
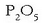 izaten dute nahaste horietan).
izaten dute nahaste horietan).
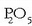 lortzeko beste modu bat
fosfato trikaltzikoa azido ortofosforoarekin erreakzionaraztea da. Horrela lortzen den superfosfatoari azido
superfosforiko esaten zaio eta %75 inguru
lortzeko beste modu bat
fosfato trikaltzikoa azido ortofosforoarekin erreakzionaraztea da. Horrela lortzen den superfosfatoari azido
superfosforiko esaten zaio eta %75 inguru
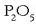 izaten dute.
izaten dute.
Ongarri potasiodunak kloruro potasikotik edo sulfato potasikotik lortzen dira. Kloruro potasioa lortzeko iturri nagusiak itsasoko ura (%0,05eko proportzioan aurkitzen baita uretan), silbina eta karnalita dira.
Ongarri bitarrak berezkoak ere izan daitezke, molekula berak bi elementuak dituelako (fosfato amonikoak, nitrofosfatoak, nitrato potasikoak edo fosfato potasikoak, adibidez). Beste batzuetan ongarri bakunak nahasten dira bitarrak lortzeko.
Gaur egun ongarri hirutarrak erabiltzen dira gehien. Garestiagoak dira, baina etekin handiagoa ematen dute eta erabil errazagoak dira. Ongarri saltzaileak lur mota bakoitzerako egokia den pr oportzioan nahastuta saltzen ditu ongarri berezi horiek.
Intsektuak hiltzeko gaiak
Nekazaritzari laguntzeko baina, ez dira nahikoak ongarriak, bai baita ongarriez ezin aurre egin dakion beste arazo bat: intsektuen izurriteak. Haiei aurre egiteko daude, beraz, intsektuak hiltzeko gaiak. Aurkitu zen lehenengoa dinitroortokresola izan zen, baina azkeneko 50 urteetan ezagunena dikloro-difenil-trikloroetanoa izan da, DDTa, alegia.
Intsektu eta bizkarroi askoren aurka ahalmen handikoa izanik ere, herrialde gehienek debekatu egin dute haren erabilera, kaltegarria baita gizakiarentzat. Intsektizida gehienak oso-oso kutsagarriak izaten dira, eta hori dela eta, 7 urtez izaten dituzte merkaturatu baino lehen probatzen, ingurunearentzat kaltegarriak diren ala ez jakiteko, horren arabera baztertu edo onartzeko.
Gai pozoidunen artean aipagarriak dira ere fungizidak.
Onddoak hiltzen dituzte, eta hedatzen galarazten. Fungizidetan ezagunena mahats eta patata
sailetan erabiltzen dena da: kobre(II) sulfatozko disoluzio bat (%2)
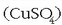 kaltzio hidroxidozko disoluzio batekin (%1)
kaltzio hidroxidozko disoluzio batekin (%1)
 nahastua.
Haziak babesteko eta desinfektatzeko oso eraginkorrak dira merkurioa duten fungizidak,
baina kontu handiarekin erabili behar dira, merkurioa oso kutsagarria baita. Ezagunena uspulum
izenaz ezagutzen dena da, merkurio ortoklorofenol sulfatoa.
nahastua.
Haziak babesteko eta desinfektatzeko oso eraginkorrak dira merkurioa duten fungizidak,
baina kontu handiarekin erabili behar dira, merkurioa oso kutsagarria baita. Ezagunena uspulum
izenaz ezagutzen dena da, merkurio ortoklorofenol sulfatoa.
Horien ordez gaur egun intsektizida organikoak erabiltzen dira, tiokarbamatoen familiakoak. Ez dira hain eraginkorrak baina ezta ere hain kutsagarriak.
Onddoak hiltzeko gai pozoidunez gainera belarrak hiltzekoak ere badira.
Horien zeregin nagusia belar mota guztiak hiltzea (errepide bazterretan edo trenbideetan, adibidez)
edo mota jakin batzuk bakarrik hiltzea (labore sailetan, adibidez) izaten da. Belar mota guztiak
hiltzen dituzten gaien artean aipagarriak dira potasio kloratoa
 eta aminotriazola
eta aminotriazola  ,
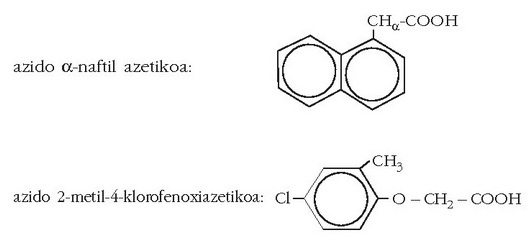
eta batzuk bakarrik hiltzen dituzten artean, berriz, azido a-naftil azetikoa
,
eta batzuk bakarrik hiltzen dituzten artean, berriz, azido a-naftil azetikoa
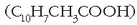 eta azido 2-metil-4-klorofenoxiazetikoa
eta azido 2-metil-4-klorofenoxiazetikoa 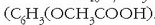
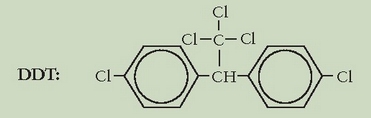
Pestizidetan ezagunena DDTa da; 1939tik aurrera asko erabili da. DDTa oso intsektizida eraginkorra da eta intsektu mota asko hiltzeko ahalmena badu ere, Anopheles eltxoaren aurka duen ahalmenagatik da batez ere ezaguna, malaria hedatzen baitu eltxo horrek. Oso gaisotasun larria izan da malaria mendeetan. Erroma klasikoaren garaian jarri zitzaion izena, latinez: mala aria (aire gaiztoa), hirian zebilen aire gaiztoren batek eragina zela uste baitzen. Plasmodium familiako bizkarroi batek eragiten du eta odolaren globulu gorriak apurtzen ditu. Gaisotasunaren zikloa luze samarra da baina gizakiok kutsatzen gaituena eltxo kutsatu baten ziztada da. Malariak badu sendabiderik baina eltxoa hiltzea da gaisotasuna ez zabaltzeko modurik hoberena. Malariaren eta eltxoek hedatzen dituzten beste gaisotasun batzuen aurrean (kalentura horia, entzefalitisa) duen eraginari esker 75 milioi gizaki salbatu direla kalkulatu da.
Zergatik du orduan horren ospe txarra DDTak? Gehiegi erabili delako, kontrolik gabe. Intsektizida gogorra dela esaten da, uzten dituen hondarrak inguruan gelditzen baitira. Ugaztunentzat oso-oso kutsagarria ez da, baina bai ordea beste izaki askorentzat (planktona, hegaztiak eta arrainak). DDTa kutsagarria zela lehen aldiz 1949an aipatu zen, baina 1962. urtean hasi zen haren aurkako kanpaina. 1972an Estatu Batuetan erabiltzea debekatu zen. Handik hara ikerketa asko egin da intsektizida eraginkorrak eta aldi berean biodegradagarriak lortu ahal izateko.
Lehergaiak
Lehergaiek, baldintza jakin batzuetan, erreakzio kimiko azkarrak eragiten dituzte eta energia
handia askatzen dute bat-batean. Adibidez: bentzeno talde bat azido nitrikoarekin erreakzioan sarrarazten bada,
oso erreakzio sendoa eta azkarra gertatzen da, eta beste konposatu batzuen artean azido pikrikoa sortzen da
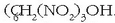 Molekula horretan dauden hiru
Molekula horretan dauden hiru 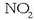 taldeek oso egongaitza bihurtzen dute. Bolbora edo sutautsa bera ere konposatu nitrogenoduna da: 75 zati nitrato potasiko
taldeek oso egongaitza bihurtzen dute. Bolbora edo sutautsa bera ere konposatu nitrogenoduna da: 75 zati nitrato potasiko
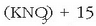 zati landare ikatz (C) + 10 zati sufre (S). Beste lehergai ospetsu bat TNT da, trinitrotolueno edo trilita
zati landare ikatz (C) + 10 zati sufre (S). Beste lehergai ospetsu bat TNT da, trinitrotolueno edo trilita

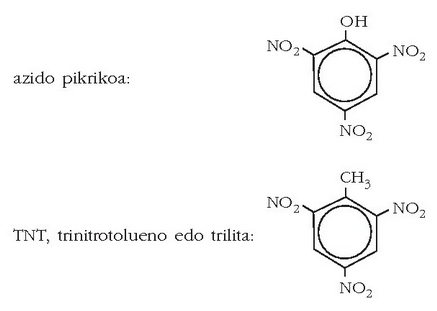
Lehergai hori nitrato amonikoarekin 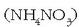 eta aluminioarekin nahastuz gero, leherketa handiak baina kontrolatuak eragiten ditu.
eta aluminioarekin nahastuz gero, leherketa handiak baina kontrolatuak eragiten ditu.
Nitroglizerina da beste lehergai ezagun bat. Glizerolaren nitrazio bidez lortzen da:
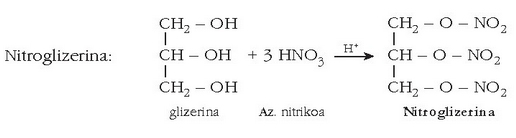
Oso arriskutsua da, mugimendu txikienak leherraraz baitezake. Dinamita ere nitroglizerinan oinarritutako lehergai bat da.
Lehergaiari, leherraraziko duen gailu bat eransten zaio, lehergarria hain zuzen. Lehergarri erabilienak fulminatoak dira, merkurio edo zilarrarenak, hots, azido fulmikoaren gatzak: CNOH.
Az. fulmikoa: O = C = N H
Azido fulmikoaren gatz bat merkurio fulminatoa da:
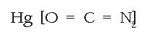
Ehunak
Gizakiak janzteko eta gorputza babesteko betidanik erabili ditu ehunak edo beste zenbait material. Historian zehar gehien erabili den zuntz naturala kotoia da. Gaur egun, ordea, gutxi erabiltzen ez bada ere, atzerakada handia egin du zuntz sintetikoen aurrean. Nolanahi ere, zuntz sintetiko askok eragiten dituzten alergiak eta dermatitisak direla eta, gero eta gehiago ari da erabiltzen berriro. Asko erabiltzen den eta oso estimatua den beste zuntz natural bat seda da (proteina zuntza da, hain zuzen ere). Lehen asmatu zen zuntz sintetikoa nylona da; 1930ean sintetizatu zen hexametilendiaminaren eta azido adipikoaren arteko erreakzioaz (ikus polimeroei buruzko gaia). Gaur egun gehien erabiltzen diren zuntz sintetikoak poliesterrak dira, polietilentereftalatoa batez ere. Zuntz akrilikoak ere oso ezagunak dira.
Zuntz sintetikoak baino lehen zuntz bitxiak lortu ziren zuntz naturala tratatuz. Horien artean ezagunena biskosa rayona izango da segur aski. Zelulosa (kotoia) sodio hidroxido eta karbono sulfuroaren laguntzaz disolbatzen da, eta zelulosa xantatoa lortzen da.
Gai hori zulo txikietatik igaroarazten da azido bainu batean, eta zelulosa sortzen da berriro, zuntz gisa orduan

